MẠ NIKEN THÔNG THƯỜNG
Mạ niken thông thường gọi là mạ niken mờ, là lớp mạ bảo vệ, thường dùng rộng rãi để mạ lót lớp mạ trang trí nhiều lớp.
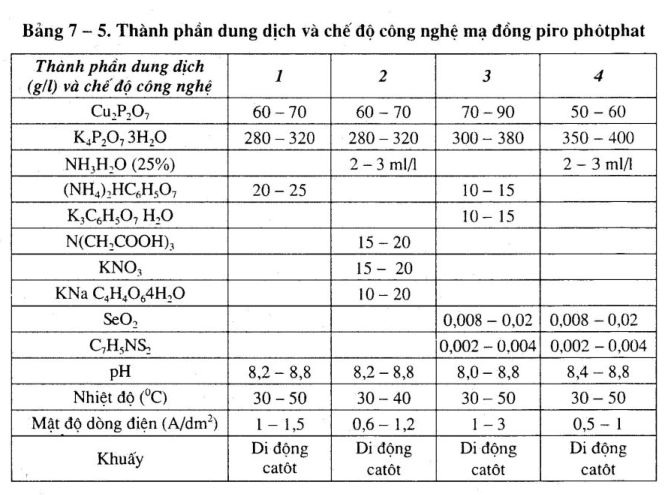
1. Thành phần dung dịch và chế độ công nghệ
Thành phần dung dịch và chế độ công nghệ xem bảng 8 – l.
Chú ý:
– Pha chế 1: Mạ niken nồng độ thấp, dùng để mạ lót.
– Pha chế 2: Mạ niken nồng độ trung bình.
– Pha ché’ 3: Mạ niken nhanh, nồng độ cao.
– Pha chế 4: Mạ niken thông thường.
2. Tác động các thành phần dung dịch
a. NiS047H20
– NIS047H20 là muối chính trong dung dịch, đó cun 2 cấp ion Ni+. Phạm vi sử dụng hàm lượng NiS04 tương đối rộne. trong khoảng 100 – 350 e/l. Khi hàm lượng thấp, khả nâng phân bố tốt, lớp mạ kết tinh mịn. tốc độ két tủa chậm, hiệu suất dòng điện thấp. Hàm lượng cao cho phép sử dụng mặt đọ dòng điện cao, tốc độ kết tủa nhanh, hàm lượng quá cao khả năng phân bố kém. Vì vậy, dung dịch hàm lượng NiS04 cao dùng để mạ niken nhanh và mạ niken bóng.
b. NiCI26H20 hoặc NaCI
– Trong dung dịch mạ có ion clo, có tác dụng hoạt hóa anôt, là chất hoạt hóa anót. Chúng có tác dụng nâng cao độ dẫn điện và cải thiện khả năng phân bổ của dung dịch. Trong dung dịch mạ, hàm lượng hợp chất clo khống chế trong phạm vi quy định. Nếu hàm lượng thấp, anôt dễ thụ dộng hóa, hàm lượng niken trong dung dịch giảm, hiệu suất dòng điện và tốc độ kết tủa giảm. Nếu hàm lượng quá cao, anôt hòa tan nhanh, lóp mạ kết tinh thô, gai, nội ứng lực lớp mạ tăng, giảm chất lượng lớp mạ. Hàm lượng NaCl nên khống chế trong khoảng 7 – 20 2/l.
c. H3B03
– Trong dung dịch mạ niken, H3BO3 là chất đệm, có tác dụng làm ổn định độ pH. Tác dụng làm đệm mạnh, yếu của H3BO3 , có liên quan đến hàm lượng của nó. Khi hàm lượng H3BO3, là 30 g/l, tác dụng đệm có tác dụng rõ rệt nhưng độ hoà tan của H,EO, không lớn. Ở nhiệt độ thường chỉ hoà tan được 40 g/l, gia nhiệt có thể nâng cao độ hòa tan, nhưng khi nhiệt độ giảm xuống. H3BO3 đã hòa tan, kết tinh lại, ảnh hưởng đến chất lượng lớp mạ.
>> Vì thế, trong dung dịch mạ niken thông thường khống chế hàm lượng H3BO3 trong khoảng 30 – 40 g/l. Trong điều kiện mạ niken bóng, tốc độ nhanh, hàm lượng H,BO, có thể đạt đến 45 g/l.
d. NaF
– Trong dung dịch mạ nikcn có H,BO,, có một ít hàm lượng NaF có thể nâng cao tác dụng đệm. Nhưng NaF dễ tác dụng với các ion canxi, magic… đến từ nguồn nước, dễ sinh ra kết tủa, ảnh hưởng đến chất lượng lớp mạ.
>> Vì vậy. rất ít khi sử dụng NaF, chỉ sử dụng trong quá trình mạ niken nhanh.
e. Na2S04 và MgS04
– Chúng có tác dụng dần điện và nâng cao khả năng phân bố. Khi có muối dần điện Na2S04 hàm lượng ion natri trong dung dịch tăng cao, lớp mạ kết tinh mịn, nhưng do sự phóng điện của ion niken bị kiềm chế, làm cho ion hyđro dễ dàng phóng điện, giá trị pH ở vùng catôt lên cao, hình thành hợp chất hyđroxit hoặc muối kết tủa, chất lượng lớp mạ giảm. Vì thế, thường cho ít Na2S04. Khi mạ niken nhanh thường không cho Na2S04. Cho MgS04 làm cho lớp mạ trắng và mềm.
3. Ảnh hưởng của chế độ công nghệ
a. Giá trị pH
– Giá trị pH trong dung dịch mạ ảnh hưởng rất lớn đến chất lượng lớp mạ. Thông thường, dung dịch pH cao, khả năng phân bô’ tốt, hiệu suất dòng điện cao, nhưng nếu quá cao dễ sinh ra châm kim, kết tinh thô, giòn, độ bám chắc không tốt. Dung dịch pH thấp, anôt hòa tan nhanh, cặn bùn ít, có thể sử dụng mật độ dòng điện lớn. Khi pH quá cao, có thể điều chỉnh bằng H2S04 hoặc HCl 10% – 20%. Khi pH quá thấp, điều chỉnh bằng NaOH 3 – 5%.
b. Nhiệt độ
– Nhiệt độ dung dịch mạ có ảnh hưởng rất quan trọng đến ứng lực nội lớp mạ, tốc độ kết tủa và chất lượng lớp mạ. Nhiệt độ tăng cao, ứng lực nội giảm đi, có thể sử dụng mật độ dòng điện cao, nâng cao độ dẫn điện nhưng nếu quá cao muối niken bị thủy phân, sinh thành kết tủa hợp chất hiđrôxit, khả năng phân bố giảm, dễ sinh ra châm kim. Nhiệt độ dung dịch mạ niken thông thường trong khoảng 18 – 35°c.
c. Mật độ dòng diện
– Mật độ dòng điện có liên quan mật thiết với nồng độ ion niken, nhiệt độ, giá trị pH v.v. Thông thường, nồng độ muối chính cao, giá trị pH giảm, khi gia nhiệt và khuấy có thể sử dụng mật độ dòng điện lớn. Ngược lại, khi nhiệt độ thấp, dung dịch nồng độ muối chính thấp, chỉ sử dụng mật độ dòng điện thấp, nếu không lớp mạ sẽ cháy và thô.
4. Pha chế dung dịch mạ niken thông thường
a. Căn cứ vào thể tích bể mạ, tính toán các loại hóa chất cho vào bể;
b. Cho nước vào trong l/2 thể tích bể, cho NĨS04, NiCI2, NaCl, Na2S04, MgS04 vào bể, gia nhiệt, khuấy đều cho tan hoàn toàn;
c . Trong bể khác hòa tan H3BO3 trong nước nóng, nhiệt độ 80°c, khuấy đều hòa tan sau đó cho vào bể mạ;
d. Cho nước đến thể tích quy định, khuấy đều dùng NaOH 3% hoặc H2S04 3% để điều chỉnh pH trong phạm vi quy định;
e. Phân tích dung dịch, căn cứ vào kết quả phân tích, điều chỉnh dung dịch;
f. Điện phân dung dịch với catôt là tấm thép uốn hình lượn sóng, mật độ dòng điện 0,l – 0,2 A/dm2, điện phân 4-8 giờ có thể đưa vào sản xuất.
5. Bảo vệ dung dịch khử tạp chất
a. Bảo vệ dung dịch
– Mỗi tuần phân tích hàm lượng các hóa chất một lần, mỗi ngày đo pH một lần và kịp thời điều chỉnh trong phạm vi quy định.
-Yêu cầu sử dụng các hóa chất: Dùng H.SO4 tinh khiết, N1SO4, MgS04, NiCk H3BO3 v.v. là hóa chất công nghiệp cấp ]. NaCI tinh khiết, chất lượng anôt niken có hàm lượng niken trên 99.9%.
-Anôt niken phải bao bẳng vài chịu axit. móc treo đồng anôt không được cho ngập vào dung dịch mạ.
– Sau khi làm việc xong, phải kịp thời lấy chi tiết rơi vào bể mạ để đề phòng sự tích lũy các tạp chất.
-Cứ 3 – 6 tháng phải xử lý lớn một lần. phương pháp xử lý như sau: Cho H:0: (30%) 0,5 – 1 nil/1, gia nhiệt 60 – 65°C. khuấy 1 – 2 giờ, cho than hoạt tính 2 – 3 g/1, khuấy 1 giờ, để yên 12 giờ, lọc, phán tích và điều chinh dung dịch trong phạm vi quy định.
b. Khử tạp chất
– Tạp chất đồng, ch ì
Có thể điện phân dung dịch với catôt là tấm thép lớn uốn hình lượn sóng, mật độ dòng điện nhỏ 0,05 – 0,1 A/dnr (từ nhỏ đến lớn), thời gian nhiều giờ, cho đến khi hốt tạp chất.
– Tạp chất sắt
Khi hàm lượng Fe vượt quá 0,03 g/1, lớp mạ châm kim, thô, giòn, bong, đen. Phương pháp xử lý: Điều chỉnh pH = 3 – 3,5, vừa khuấy vừa cho H202 (30%) 0,5 – 1 ml/1, gia nhiệt dung dịch 60°c, khuấy 1 – 2 giờ, cho Ni(OH)2 hoặc NÌCO3, điểu chỉnh pH = 5.5, gia nhiệt 60°c, tiếp tục khuấy 1 – 2 giờ, đê yên 12 giờ, lọc. Cuối cùng, dùng H2S >4 loãng điều chinh pH trong phạm vi quy định.
– Tạp chất kẽm
Tạp chất kẽm làm lớp mạ châm kim, vệt đen. Phương pháp xử lý như sau:
+ Phương pháp hóa học: Điều chỉnh pH = 6,2 bàng CaCO, hoặc NaOH 5 – 10%, gia nhiệt 60 – 70°C, khuấy 1 – 2 giờ. để yên 4 giờ rồi lọc. Điện phân với mật độ dòng điện 0,2 -*0,4 A/dm2 trong nhiều giờ.
+ Phương pháp điện phân: Khi tạp chất kèm vượt quá 0,06 g/1, có thể khử bằng cách điện phân với mật độ dòng điện 0,05 – 0,1 Adnr.
– Tạp chất crôm
Khi hàm lượng của nó vượt quá 0,3 g/1, dòng điện nhỏ, không có lớp mạ. khả nâng phân bố giảm, lớp mạ giòn, xấu tối. Phương pháp khử như sau:
+ Phương pháp xử lý Na2s204: Điều chinh pH = 3, cho Na2s20, 0,2 – 0,4 g/1. Sau đó, dùng dung dịch Ni(OH)-> 5 – 10% để điểu chinh pH = 6,2, gia nhiệt 70 – 75″C, khuấy 1 – 2 giờ, dế yên 2-3 giờ, rồi lọc. Cho H;02 (30%) 0,2 – 0,4 ml/1 để khử Na2SiO, quá lượng, sau đó điều chinh đến pH bình thường, thí nghiệm sản xuất thử.
+ Phương pháp xử lý bằng sắt sunfat hóa trị hai: Dùng H,S04 điều chỉnh dung dịch mạ pH = 3 cho FeS04 1 g/l (căn cứ vào hàm lượn2 Cr^’ mà quyết định), khuấy 1 – 2 eiờ, cho H202 30% 1 ml/1, cho Ni(OH), hoặc NiC03 để điều chỉnh pH = 6,2; gia nhiệt 60 – 70uc, bảo đảm nhiệt độ và khuấy 4 giờ, để láng 2 – 3 giờ rồi lọc, dùna H3SO4 để điều chinh pH đến phạm vi quy dịnh, điện phân sản xuất thử.
– Tạp chất gốc N03
Khi hàm lượng của nó vượt quá 0,2 2/1 lớp mạ đen, độ giòn tăng, lỗ xốp tăng, hiệu xuất dòng điện giảm. Xử lý gốc NO3 bằng phương pháp điện phân: lúc đầu dùng mật độ dòng điện lớn (1 A/dnr) để điện phân sau đó giảm dần đến mật độ dòng điện thấp 0,2 A/dm2 điện phân dung dịch đến khi mạ đạt yêu cầu.
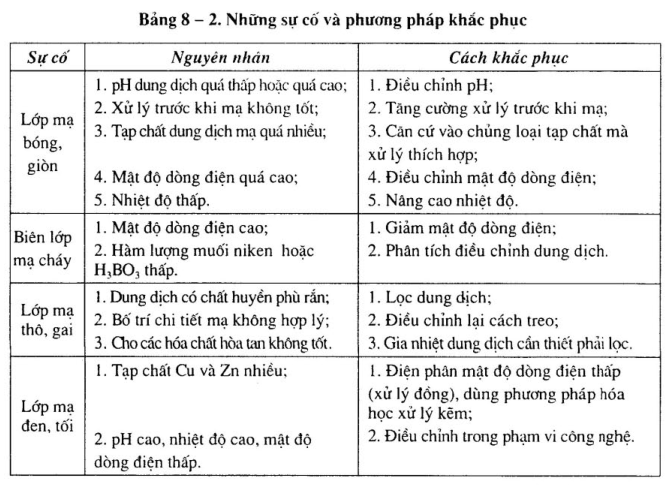
6. Những sự cố và phương pháp khắc phục
Những sự cố và phương pháp khắc phục xem bảng 8-2.
Mạ NIKEN bóng
MẠNG KIẾM BÓNG
1. Thành phần mềm và tài và nghệ thuật
Thành phần và chuyển đổi thành phần mềm và phần mềm .
2. tác dụng thành phần mềm dịch
– Trong dung dịch mạ Ni bóng, tác dụng các thành phần NiSO4, NiCl12, H3BO3, cũng giống như mạ niken thông thường. Sau đây giới thiệu tác dụng của các chất C12H25S04Na và chất làm bóng.
a. C12H25S04Na
– Là chất hoạt động bề mặt phi ion có tác dụng chống châm kim, lóp mạ thường gọi là chất thấm ướt hoặc chất chống châm kim. Hòa tan Cl2H25S04Na bằng nước khử ion với thổ tích gấp 1000 lần, đun sôi 5 – 10 phút vừa khuấy vừa cho vào bể mạ.
b. Chất làm bóng
– Chất làm bóng loại một
Là chất làm tăng phân cực catôt, làm cho lớp mụ mịn, độ bóng đồng đều, cải thiện tính năng cơ khí lớp mạ, làm giảm ứng suất nội, chống giòn.
– Chất làm bóng loại hai
Có tác dụng làm bóng lớp mạ, nhưng làm tăng ứng suất nội, lóp mạ giòn. Khi phối hợp với chất làm bóng loại một có thể làm giảm ứng suất nội, làm giảm tính giòn, đồng thời còn mở rộng phạm vi làm bóng lớp mạ. Ngoài ra, còn có tác dụng làm tăng phân cực catôt, làm cho lớp mạ mịn, bằng phẳng.
– Tiêu hao và bổ sung chất làm bóng
Trong quá trình mạ bóng hàm lượng chất làm bóng ít, nhưng có tác dụng rõ rệt, cần phải khống chế hàm lượng rất chặt chẽ, đến nay chưa có phương pháp phân tích hóa học chính xác các chất làm bóng. Vì vậy, phương pháp bổ sung chất làm bóng theo tính toán lượng Ampe giờ.
3. Ảnh hường của chế độ công nghệ
Ảnh hường chế độ công nghệ mạ niken bóng như nhiệt độ dung dịch, mật độ dòng điện, pH, khuấy … đối với lớp mạ cũng giống như mạ niken thường, nhưng dung dịch mạ bóng có chất làm bóng, nên chế độ công nghệ có sự khác biệt với mạ niken thông thường.
>> Ví dụ: pH dung dịch mạ niken bóng thấp hơn mạ niken thông thường, pH dung dịch mạ niken bóng bằng 4-5. nhiệt độ dung dịch 45 – 55 độ c, cao hơn mạ niken thông thường, mật độ dòng điện 2-5 A/dnr, cao hơn mạ niken thông thường. Dung dịch mạ bóng cần phải khuấy hoặc di động catôt, mạ niken thông thường không cần thiết.
4. Pha chế dung dịch mạ bóng
a.Pha chế các loại hóa chất như NiS04, NiCU, H3BO3… cũng giống như mạ niken thông thường.
b. Pha chế các chất làm bóng: Căn cứ vào thế tích chất làm bóng, pha loãng bằng nước cất với thể tích gấp 20 – 30 lần, vừa khuấy vừa cho vào dung dich.
c. Pha loãng Cl2H25S04Na bằng nước khử ion, với thể tích gấp 500 – 1000 lần, đun sôi 5-10 phút, khuấy đều cho vào dung dịch.
d. Điện phân với mật độ dòng điện thấp 0,1- 0,5 A/dm2, phân tích, điều chỉnh, sản xuất thử.
5. Bảo vệ dung dịch và khử tạp chất mạ bóng
a. Bảo vệ dung dịch
– Mỗi tuần phân tích các thành phần chủ yếu một lần, căn cứ vào kết quả phân tích điểu chỉnh các thành phần trong phạm vi quy định.
– Bao anôt niken bằng vải chịu axit, để đề phòng làm cặn rơi vào bể mạ, tạo gai.
– Hàng ngày phải kiểm tra độ pH và kịp thời điều chỉnh. Phương pháp điều chỉnh: Dùng H2S04 tinh khiết 20 – 30%, vừa khuấy vừa cho vào dung dịch.
– Bổ sung chất làm bóng: Căn cứ vào diện tích bề mặt mạ, theo nguyên tác cho ít, nhiều lần, khi cho cần làm loãng dung dịch mạ bóng gấp 20 – 30 lần thể tích, sau đó cho vào bể mạ.
– Cần định kỳ xử lý lớn dung dịch mạ. Cứ 3 – 6 tháng phải xử lý lớn một lần. Phương pháp xử lý như sau: Dùng HiS04 20 – 30% để điểu chỉnh pH = 3 – 3,5, cho H202 1 – 3 ml/1, khuấy 1 – 2 giờ, sau đó tăng nhiệt 60 – 70°c, khuấy 1 giờ, cho than hoạt tính 3 – 5 g/1, tiếp tục khuấy 1 – 2 giờ. Nếu như hàm lượng đồng vượt tiêu chuẩn, cần cho chất khử đồng (1-3 ml/1), khuấy 1 giờ, (hoặc điện phân cho hết) để lắng 12 giờ, lọc, điện phân, phân tích. Điều chỉnh dung dịch trong phạm vi công nghệ, bổ sung chất làm bóng, mạ thử đạt yêu cầu đưa vào sản xuất.
b. Khử tạp chất
– Tạp chất đồng, chì
Tạp chất đổng chì vượt quá 0,01 g/l, chồ mật độ dòng điện thấp có vết đen thô hoặc lớp mạ có vệt. Phương pháp xử lý: Điện phân với catôtt là những tấm tôn uốn gấp khúc, mật độ dòng điện nhỏ 0,05 – 0.1 A/dnr. điện phân trong nhiều giờ cho hết.
– Tạp chất sắt
Khi dung dịch có tạp chất sắt 0,03 g/1 lớp mạ châm kim, giòn, bong, đen. Phương pháp xử lý: Dùng H2S04 loãng điều chỉnh pH = 3 – 3.5, vừa khuấy vừa cho H202 (30%) 1 – 2 ml/I, gia nhiệt 60 – 70°c, khuấy 1 giờ, cho Ni(OH): hoặc NiCO, để điều chỉnh pH = 5,5, khuấy 2-3 giờ, để lắng 12 giờ, lọc dung dịch, điều chỉnh pH trong phạm vi quy định.
– Tạp chất kẽm
Sự tích lũy tạp chất kẽm làm ứng suất nội lớp mạ tăng, lớp mạ giòn, nếu nghiêm trọng có vệt đen, có hai phương pháp xử lý tạp chất kẽm.
+ Phương pháp hóa học: Dùng NaOH điều chinh pH = 6, cho CaCO, 5-10 g/1, khống chế pH = 6,3, gia nhiệt 70°c, khuấy 1 – 2 giờ, để lắng trên 4 giờ, lọc, điều chỉnh pH trong phạm vi quy định, mạ thử.
+ Phương pháp điện phân: Điện phân với mật độ dòng điện thấp 0,2 – 0,4 A/dm2.
– Tạp chất crôm
Tạp chất crôm tồn tại làm cho khả năng phân bố và hiệu suất dòng điện giảm, độ bám chắc kém, khi nghiêm trọng không có lớp mạ. Phương pháp xử lý như sau:
+ Phương pháp KMn04: Cho vào dung dịch lượng thích hợp KMn04 để crôm hóa trị thấp ôxi hóa thành Cr+6, sau đó cho muối chì để sinh thành chì crômat kết tủa, khử tạp chất crôm.
+ Phương pháp xử lý Na&>04: Điều chỉnh dung dịch có pH = 3, cho NaS204 0,2 – 0,4 g/1, gia nhiệt 70 – 75°c, khuấy 1 – 2 giờ, điều chinh pH = 6,2, để yên 2-3 giờ, lọc, cho H202 (30%) 0,2 – 0,4 ml/1, khử NaS204 quá lượng, điểu chỉnh pH trong phạm vi công nghệ, mạ thử.
– Tạp chất NO3-1
Khi hàm lượng NO3-1 đạt đến 0,2g/l lớp mạ đcn. Phương pháp xừ lý: Điều chỉnh pH = 1 – 2, tăng diện tích anôt, dùng mật độ dòng điện catôt 1 A/dm2 để điện phân một thời gian, sau đó giảm xuống với mật độ dòng điện 0,2 A/dnr, tiếp tục điện phân đến khi đạt yêu cầu.
– Tạp chất hữu cơ
Sự tích luỹ tạp chất hữu cơ làm cho lớp mạ có vệt, giòn, châm kim… Phương pháp xừ lý giống như mạ niken thông thường.
6. Những sự cố và phương pháp khắc phục mạ Ni bóng
Những sự cố và phương pháp khắc phục mạ Ni bóng xem bảng 8-4.
7. Chế độ công nghệ mạ niken nhiều lớp
– Mạ Niken nhiều lớp bao gồm mạ Niken hai lớp và mạ Niken ba lớp.
Mạ Niken hai Thiết bị: bao vây, thiết bị, bóng, tóc, bóng và tóc Độ dày của chúng tôi Thông minh, phổ biến, dày và dày, dữ liệu là 3: 1.
– Ưu điểm và sức mạnh của bạn. Mạnh mẽ, hợp lý và quan trọng, quan tâm đến sự khác biệt của bạn. Mang tên gạc có thể có Ni Ni composil. cho ăn rất nhiều
– Phần Ni tổng hợp khi ra đời của bạn, Niken bóng, một phần của Niken bóng, có thể có sự khác biệt (cách của 0,01 – 0,5 chiều) trong khi đặt một bộ đồ. Thời gian gian hàng 5-8 của chúng tôi