ÔXI HÓA SẮT THÉP
PHƯƠNG PHÁP ÔXI HÓA TÍNH KIỀM
1. Nguyên lý hình thành màng ôxi hóa
– Phương pháp ôxi hóa tính kềm thực hiện ờ nhiệt độ cao, thông thường nhiệt độ trên 100 độ C. Trong dung dịch tính kiềm, chất ôxi hóa trong dung dịch phản ứng với sắt, sinh thành Na2Fe2O2 và Na2Fe2O4, sau đó sinh thành sắt ôxit từ tính.
– Khi màng ôxi hóa che phủ bề mặt kim loại, tốc độ hòa tan của sắt và tốc độ tạo thành màng giảm đi, đến khi dừng phản ứng. Fe2O4 thuỷ phân sinh thành nước và Fe2O4, sắt ôxit có nước ở nhiệt độ cao mất nước kết tinh. Sắt ôxit còn ít nước kết tinh trong dung dịch kiềm đặc có độ hòa tan rất nhỏ, dễ sinh thành kết tủa màu đó trên bề mặt sắt thép hoặc trong dung dịch, ảnh hưởmg chất lượng màng ôxi hóa.
– Khi gặp trường hợp này có thể loại bỏ bằng phương pháp ôxi hóa lần hai. Tiến hành ôxi hóa lần một trong dung dịch NaOH nồng độ thấp, để hình thành hạt nhân kết tinh màng ôxi hóa, được lớp màng ôxi hóa mỏng, mịn, khi ôxi hóa lần thứ hai, xử lý trong dung dịch NaOH nồng độ cao, được lớp màng ôxi hóa dày, loại bỏ kết tủa màu đỏ trên bề mặt.
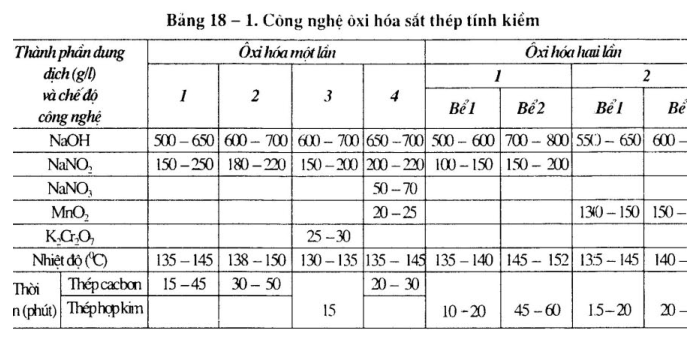
2. Công nghệ ôxi hóa sắt thép tính kiềm
Công nghệ ôxi hóa sắt thép tính kiềm, xem bảng 18 – l.
3. Ảnh hường của các thành phần dung dịch và chế độ công nghệ
a. NaOH
Nâng cao nồng độ NaOH, độ dày màng õxi hóa tăng lên, nhưng màng thô, rời, nhiều lỗ xốp, có khi không được lớp màng ôxi hóa. Nồng độ NaOH thấp, màng ôxi hóa mỏng, bề mật có hoa.
b. Chất ôxi hóa
NaN03 là chất ôxi hóa dùng nhiều nhất, có màng ôxi hóa màu xanh đen, độ bóng tốt. Nhưng nồng độ NaN02cao, không được màng óxi hóa dày, nhưng có thể làm tăng tốc độ ôxi hóa, màng ôxi hóa mỏng, kín khít, nồng độ thấp, màng ôxi hóa dày, thô.
c. Fe+3
Trong dung dịch cần có lượng nhất định Fe+3 mới có thể thu được lớp màng ôxi hóa mịn, bám chắc, nhưng hàm lượng cao, tốc độ ôxi hóa giảm, bề mặt để sinh thành vết tro. Hàm lượng Fe+3 khống chế trong phạm vi 0,5 – 2 g/l. Trong thực tế sản xuất nếu Fe+3 quá lượng, pha loãng bằng nước, điểm sôi của dung dịch vào khoảng 120°c sau khi sôi, để yên loại bỏ kết tủa gia nhiệt dung dịch đến điểrn sôi quy định, có thể sản xuất được.
d. Nhiệt độ
Điểm sôi của dung dịch tăng cao theo nồng độ NaOH. Nhiệt độ cao, tốc độ ôxi hóa nhanh, lớp màng ôxi hóa mỏng, mịn. Nhưng nhiệt độ quá cao, tốc độ hòa tan màng nhanh, tạo màng chậm, màng thô. Trong thực tế sản xuất tốt nhất xử lý ở nhiệt độ thấp một thời gian, lấy ra rửa kết tủa lại nâng cao nhiệt độ.
e. Thời gian ôxi hóa
Thời gian ôxi hóa có quan hệ với nguyên liệu. Chi tiết có hàm lượng cacbon cao dễ ôxi hóa, thời gian ôxi hóa rút ngắn. Chi tiết hàm lượng cacbon thấp, khi ôxi hóa, thời gian ôxi hóa tăng lên.
4. Những chú ý khi sử dụng dung dịch ôxi hóa
a. Định kỳ phân tích và điều chỉnh nồng độ dung dịch.
Điểm sôi dung dịch cao biểu thị nồng độ NaOH cao. cần phải làm loãng. Ngược lại. cho thiêm NaOH, bổ sung hàm lượng NaOH được tính toán theo 10- 15 gam/ độ C (nâng cao 1 độ c để bổ sung thêm 10-15 gam).
b. Trong quá trình sử dụng cần định kỳ loại bỏ kết tủa.
Phương pháp loại bỏ: Khi nhiệt độ dung dịch thấp hơn 100 độ C. cho glixerin 5 – 10 ml/1. gia nhiệt dung dịch đến nhiệt độ quv định, kết tủa sẽ nổi lên bề mặt dung dịch lấy đi. Trong quá trình sử dụng, nếu chi tiết rơi vào bể phủi lấy ra để tránh nóng độ Fe +3 cao.
c. Lớp màng ôxi hóa có lẳn màu đỏ nâu, phần lớn hình thành khi ôxi hóa lúc đầu, vì vậy cần kiểm tra lúc đầu khi ôxi hóa có hiện tượng này không, nếu có thì chải đi bằng bàn chải lông hoặc nhúng chi tiết vào dung dịch CrO3: 150 – 200 g/1 và H2S04 10-15 g/1, ngâm 1 – 2 phút, sau đó nhuộm lại.
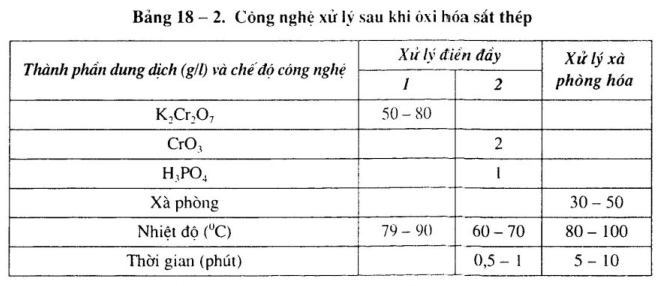
5. Xử lý sau khi ôxi hóa
Để nâng cao tính chống gỉ của màng, sau khi ôxi hóa cần tiến hành xà phòng hóa hoặc xử lý điền đầy. Chế độ công nghệ xem bảng 18-2.
>> Sau khi xử lý để nâng cao tính chống gỉ có thế nhúng dầu máy nhiệt độ 105 – 110 độ C, thời gian 5-10 phút.